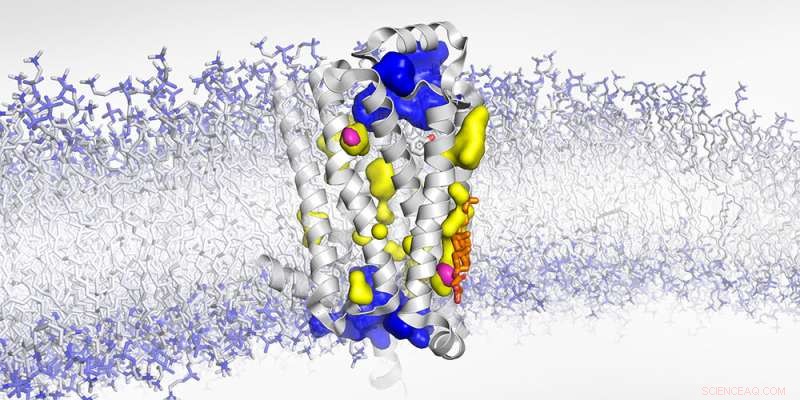
Struktur av den membranbundna β1-adrenerga receptorn med vattenexponerade håligheter (blå), oåtkomliga för vatten (gul) och torra tomrum (magenta). Kredit:Biozentrum, University of Basel
Nästan alla vitala funktioner i människokroppen regleras av så kallade G-proteinkopplade receptorer på cellytan. Dessa receptorer fungerar således som attraktiva läkemedelsmål för att behandla olika sjukdomar. Forskare har nu upptäckt att tomma utrymmen inuti dessa receptorer är viktiga för deras aktivering och därmed för att förmedla meddelanden till den inre cellen. Deras tillvägagångssätt för att lokalisera dessa tomrum kan hjälpa till att styra sökandet efter nya droger.
De G-proteinkopplade receptorerna (GPCR) gör att vi bland annat kan se, smaka på mat, känna oss kalla eller varma eller svara på stress. Beläget på cellytan känner GPCR:er av en mängd olika signaler såsom näringsämnen, ljus, lukter eller hormoner. Genom att ändra sin konformation överför de denna information från utsidan till insidan av cellen. Den samlade kunskapen om GPCR har oerhört påverkat modern medicin:ungefär en tredjedel av alla marknadsförda läkemedel riktar sig mot GPCR.
Tömma utrymmen som är viktiga för receptoraktivering
Med hjälp av den senaste tekniken har forskargruppen under ledning av Prof. Stephan Grzesiek, tillsammans med medarbetare vid Biozentrum vid universitetet i Basel och Paul Scherrer Institute, nu upptäckt att GPCR innehåller helt tomma håligheter som är viktiga för deras aktivering. Deras senaste, experimentella tillvägagångssätt, publicerad i Nature Chemistry , kan styra och påskynda sökandet efter nya och mer specifika läkemedelskandidater med färre biverkningar.
Även om de 826 GPCR i människokroppen svarar på många olika stimuli, delar de alla en gemensam arkitektur. "Vårt mål är att på atomär nivå förstå hur GPCR:er sänder signaler", säger Dr Layara Abiko, som ledde studien. "I många år har vi därför studerat den β1-adrenerga receptorn, en GPCR som förbereder kroppen för kamp eller flykt." Hormonet adrenalin binder till och aktiverar receptorn som utlöser en stressreaktion, till exempel, vilket orsakar en ökning av hjärtfrekvens och blodtryck." Betablockerare hämmar denna receptor och är därför effektiva läkemedel för att behandla högt blodtryck eller hjärt-kärlsjukdomar.
Exakt lokalisering av torra tomrum
"Tack vare högtrycks-NMR och vårt experimentella tillvägagångssätt med röntgenspridning på receptorkristaller som inkorporerade ädelgasen xenon, kunde vi ytterligare komplettera bilden av denna mycket dynamiska receptor", säger Abiko. "Tidigare antog man att hålrummen inuti receptorn är fyllda med vatten. Vi har nu avslöjat att några av dem är tomma." Under aktivering förändras receptorns konformation på ett sådant sätt att dessa torra hålrum komprimeras och försvinner. Följaktligen krymper receptorn precis som när du klämmer på en svamp. När det gäller den β1-adrenerga receptorn är denna konformationsförändring nyckeln för att initiera kroppens kamp-eller-flykt-svar.
Forskarna har nu kunnat exakt lokalisera två av sådana tomma hålrum och avslöjat att kolesterol – en viktig cellmembrankomponent – kan fylla en av dessa. Som en kil hindrar kolesterol receptorn från att klämmas och ändras till dess fullt aktiva tillstånd. "Att blockera detta tomrum hindrar de subtila, men väsentliga rörelserna som krävs för att aktivera GPCR", förklarar Abiko. "Vi tror att den här kileffekten kan vara ytterligare ett lager av receptorreglering."
Nya vägar för läkemedelsutveckling
Men varför kan det vara viktigt att spana efter torra tomrum? Klassiska läkemedelsbindningsställen är ofta liknande bland GPCR-underklasser. Ett läkemedel riktat till ett sådant ställe kan binda till mer än en receptor och därför orsaka oönskade biverkningar. Däremot skiljer sig de torra kaviteterna avsevärt mellan GPCR, även när de är från samma underklass. Detta gör dem till mycket selektiva läkemedelsmål.
"På detta sätt kan du designa läkemedel som är mycket specifika för en receptor", förklarar Abiko. Den utvecklade nya metoden kan lokalisera sådana okonventionella läkemedelsbindningsställen som skiljer sig starkt mellan receptorerna. Detta kan hjälpa screeningprocessen för nya terapier, spara tid och minska kostnaderna. + Utforska vidare