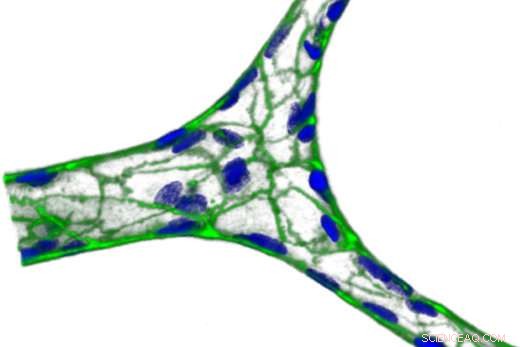
Ett blodkärl i miniatyr, bildad på agaros/gelatinhydrogel. Grön representerar VE-cadherin, ett protein som limmar ihop celler, och blått är kärnor. Kredit:Yongzhi Qiu
Vid sjukdomar som malaria och sicklecellssjukdom, röda blodkroppar bryts ner, med skadliga effekter på resten av kroppen – särskilt slemhinnan i små blodkärl.
Biomedicinska ingenjörer har etablerat ett modellsystem för att studera dessa problem, som har potential att användas även vid andra hjärt-kärlsjukdomar. Systemet bygger ett nätverk av konstgjorda blodkärl, baserat på välbekanta "hydrogel"-material som löses upp med värme:gelatin och agaros, ett socker som härrör från tång.
Resultaten publicerades nyligen av Nature Biomedicinsk teknik .
"Den viktigaste tekniska innovationen här är att vår hydrogel kan hålla dessa kärl växande i veckor till månader, som är mycket längre än standardmetoder, " säger seniorförfattaren Wilbur Lam, MD, Ph.D. "Med detta system, vi kan studera inte bara hur kärl reagerar på aspekter av sjukdom utan också hur väl kärlen kommer att läka över tiden när dessa förolämpningar har tagits bort."
Lam är biträdande professor vid avdelningen för pediatrik vid Emory University School of Medicine och på Wallace H. Coulters avdelning för biomedicinsk teknik vid Georgia Tech och Emory University.
Jobbar med Lam, instruktör Yongzhi Qiu, Ph.D. och kollegor konstruerade en hydrogelbaserad mikrofluidisk enhet, med förgreningskärl ungefär 20 mikrometer tvärs över. Enheten kan sedan beläggas med endotelceller, som kantar blodkärlen, och ansluten till en pump. En fördel med att använda hydrogeler, författarna skriver, är att hydrogeler inte är lika styva som fasta polymerer, och svarar således på ett mer fysiologiskt relevant sätt på förändringar i vätskeflödet.
När den väl är färdigmonterad, endotelcellerna försvagar sina barriärer som svar på inflammatoriska molekyler som TNF-alfa och läker sedan efteråt.
Forskarna testade också svar på hem, en komponent av hemoglobin som bildas när röda blodkroppar bryter upp, och de testade effekterna av ocklusionsbenägna röda blodkroppar från patienter med sicklecellsjukdom och röda blodkroppar infekterade av Plasmodium-parasiter.
Modellsystemet skulle kunna användas för att ytterligare dissekera effekterna av röda blodkroppar kontra andra celler och inflammatoriska molekyler, och screening för läkemedel som kan förhindra skador på blodkärl, säger forskarna.