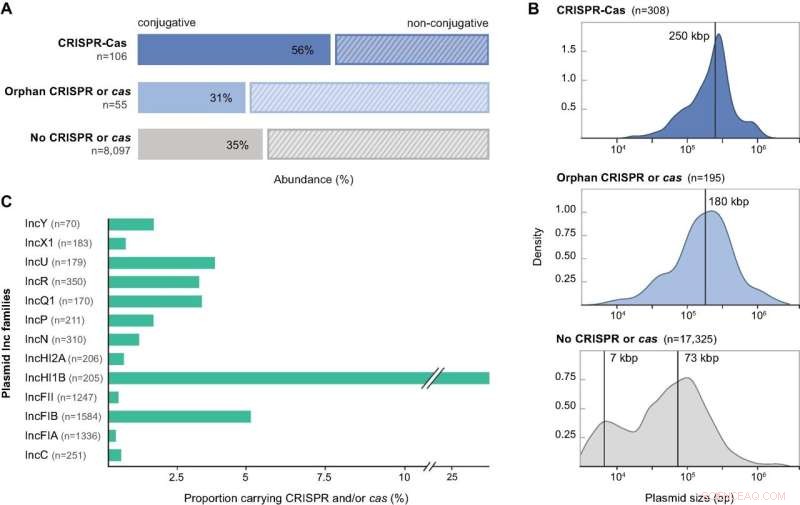
Funktioner hos plasmider som kodar för CRISPR-Cas-komponenter. (A) Rörlighetsförutsägelser för insamlingen av icke-redundanta proteobakteriella plasmider som analyserats i denna studie, presenterade enligt deras CRISPR-Cas-innehåll:kompletta CRISPR-Cas-loci, orphan CRISPRs eller cas, och ingen CRISPR eller cas. (B) Storleksfördelningar för insamling av plasmidgenom som bär kompletta CRISPR-Cas loci, orphan arrays, solo cas-operoner och inga CRISPR- eller cas-gener. Vertikala linjer indikerar medianplasmidstorleken för de unimodala fördelningarna och uppskattade medelvärden från en 2-komponent gaussisk blandningsmodell för den bimodala fördelningen. Densiteter beräknas med standardparametrar i bas R. (C) Fördelning av plasmidinkompatibilitetsgrupper inom den Inc-typbara fraktionen av den kompletta plasmiddatauppsättningen och relativ förekomst av delmängden som kodar för CRISPR-Cas loci. Enstaka plasmider kan tillhöra mer än en Inc-grupp. Endast Inc-grupper som innehåller mer än 10 plasmider visas. Kredit:Nucleic Acids Research DOI:10.1093/nar/gkab859
CRISPR-Cas har blivit något av en superstjärna under det senaste decenniet som ett genredigeringsverktyg med revolutionerande potential, särskilt inom hälsovetenskap. Ursprungligen känt som ett immunförsvar i bakterier, naturligt förekommande CRISPR-Cas har visat sig vara mer mångsidigt och mångsidigt till sin natur än vad forskare en gång trodde. Nu har en grupp forskare vid Köpenhamns universitets Biologiska institution undersökt förekomsten av CRISPR-Cas-system i plasmider.
Forskarna undersökte mer än 30 000 kompletta plasmidgenom och fann CRISPR-Cas i cirka tre procent av dem - en hög andel även jämfört med bakterier. De hittade också olika representanter för så många som fem av de sex kända typerna av CRISPR-Cas i de studerade plasmidgenomen. Resultaten visar att CRISPR-Cas-system är både utbredda och mångsidiga i plasmider och, intressant nog, att de allra flesta av dem riktar sig mot andra plasmider.
"Delvis är detta spännande eftersom det stöder en nyare förståelse av plasmider som har en högre grad av autonomi från sina värdceller, vanligtvis bakterier. Men också, eftersom det i det långa loppet kan öppna vägar för att bekämpa virulens och resistens. i bakterier, vilka plasmider hjälper till att spridas", förklarar Rafael Pinilla-Redondo, som är en av studiens huvudforskare och baserad vid Köpenhamns universitets biologiavdelning.
CRISPR fungerar som en genomisk GPS, där ett lagrat minne av främmande DNA-fragment kan användas för att lokalisera ett mål för Cas-proteiner, den "genetiska saxen". I majoriteten av studiens fynd var det DNA från andra plasmider som upptäcktes i immunminnet hos CRISPR-Cas-systemen – dvs. placeras i hårkorset.
En del av ett paradigmskifte
Enligt forskarna tyder detta på en kamp om resurser bland plasmider, där plasmider tjänar sina egna intressen genom att aktivt arbeta för att förhindra att andra plasmider kommer åt värdbakterien där de finns. I den här striden använder de CRISPR som ett vapen.
Forskarna hade möjlighet att samtidigt undersöka värdbakterierna i 30 000+ plasmiddataset för samma CRISPR-Cas-sekvenser. Tanken var att studera om de sekvenser som hittats i plasmider speglade CRISPR-innehållet i värdceller, men detta var i allmänhet inte fallet.
"Våra fynd tyder på att plasmider har en hög grad av autonomi från bakterierna där de lever. Även om plasmider är beroende av sin värd, är de också genetiskt oberoende enheter som tjänar sina egna intressen. Deras olika CRISPR-Cas-innehåll är ett bra exempel på denna autonomi", säger Rafael Pinilla-Redondo.
De nya forskningsresultaten kommer att bidra till vad forskarna anser vara ett paradigmskifte inom mikrobiologi. Inom mikrobiologi avser genflöde eller genöverföring när genetiskt material rör sig mellan celler, förmedlade mobila genetiska element. Medan vissa mobila genetiska element tillåts glida in, till fördel för en cell, stoppas andra eftersom de är skadliga. Den allmänna uppfattningen har länge varit att bakterier styr genflödet.
Paradigmskiftet pekar på en förståelse där bakterier faktiskt spelar en mycket mindre viktig roll för att påverka genflödet.
"Det som en gång antogs vara bakterier som kämpade för att skydda sig mot genetiska parasiter, som virus och plasmider, är mycket mer komplext. Kanske borde det förstås bättre som att parasiterna kämpar sinsemellan, till exempel om vilka som ska tillåtas att leva bakom en kos öra", förklarar Rafael Pinilla-Redondo.
Möjligheten till nya vapen mot antibiotikaresistens
Den nya kunskapen om hur plasmider använder CRISPR kan påverka hur vi bekämpar farliga bakterier i framtiden. Plasmider är nyckeln till spridningen av skadliga gener mellan bakterier genom vad som kallas horisontell genöverföring.
Spridningen av genetiskt material är avgörande för bakteriers förmåga att anpassa sig till nya miljöer och utmaningar. Från en antibiotikaresistent bakterie kan en plasmid kopiera sig själv och överföra den egenskapen till omgivande bakterier som en del av sitt eget DNA.
Som sådan kan strider mellan plasmider hjälpa forskare att lära sig mer om hur man bekämpar dem också.
"Genom att förstå hur plasmider konkurrerar sinsemellan kan vi kanske lära oss att bromsa dem och därigenom bromsa spridningen av antibiotikaresistens och virulenta, skadliga egenskaper mellan bakterier", säger Søren Johannes Sørensen, professor i mikrobiologi och medförfattare till forskningsartikeln.
"På lång sikt är det möjligt att vi kommer att kunna göra plasmidernas strategier till våra egna och använda dem som verktyg. Utan att låna från naturen skulle vi vara ganska begränsade. Men om vi kan lära oss om styrkorna och svagheterna med plasmider från dem själva, kommer möjligheter att dyka upp", säger han.
Vad betyder CRISPR-Cas?
DNA-fragment (CRISPR) och Cas-proteinsax (t.ex. Cas9) kan lokalisera specifika DNA-sekvenser och klippa dem.
Det förutspås att CRISPR-Cas kommer att spela en revolutionerande roll som ett genredigeringsverktyg, inte minst inom hälsovetenskapen, för behandling av bland annat genetiska sjukdomar.
CRISPR-system sågs ursprungligen som ett immunsystem för bakterier, särskilt mot virus. Men många forskare ser nu CRISPR-Cas som ett "guns for Hire"-verktyg som kan användas för en mängd olika ändamål, av många olika aktörer, inklusive bakterier, plasmider – och människor.
Vad är en plasmid?
En plasmid är en liten ringformad DNA-molekyl, ett så kallat mobilt genetiskt element, som finns i bakterier och vissa andra typer av mikroorganismer.
Det påminner om virus, eftersom båda är parasiter i celler. Plasmider kan reproducera sig oberoende av värdcellen och ger ofta fördelar för värdcellen.
De kan bland annat ge eller överföra genetiska egenskaper till en bakterie, till exempel genom att göra den antibiotikaresistent eller patogen, i en process som kallas horisontell genöverföring.
Plasmider har länge varit ett viktigt verktyg inom molekylärbiologin för bland annat genkloning och införande av genetiskt material i bakterieceller.
Vad är horisontell genöverföring?
Horisontell genöverföring är när en organism överför gener till en annan organism som inte är dess egen avkomma.
Bakteriers förmåga att anpassa sig till nya miljöer och utmaningar beror till stor del på tillgången på nya gener på detta sätt.
Fenomenet är ansvarigt för den hotande antibiotikaresistenskrisen, eftersom bakterier snabbt utvecklar resistens mot antibiotika genom att förvärva resistenta gener. Det förmedlas mycket ofta av plasmider, vilket gör plasmidproliferation till ett globalt folkhälsoproblem.
Om studien:Forskare skapade en CRISPR-skanner
För att studera förekomsten av CRISPR-Cas i plasmider använde forskarna den största samlingen av fullständigt sekvenserade plasmidgenom, en datauppsättning sammanställd av forskare runt om i världen.
För att hantera de rejäla mängderna data utvecklade forskare från Institutionen för biologi programvara för att skanna efter kända CRISPR-delar. Programmet, som heter CRISPRCasTyper, har sedan dess gjorts fritt tillgängligt för andra forskare. + Utforska vidare