
Bild på forskarna, med (från vänster till höger):Dr. Hen Dotan, Avigail Landman, Prof. Avner Rothschild, Prof. Gideon Grader. Kredit:Chen Galili, Technions talespersonavdelning.
Elektrolytisk väteproduktion innebär generering av väte från vatten med hjälp av elektrisk kraft, som helst ska komma från förnybara kraftkällor som solljus och vind. Även om denna metod för att producera väte kan vara en mycket lovande lösning för att öka hållbarheten, men forskare måste övervinna flera viktiga utmaningar för att det ska bli utbrett.
I en nyligen genomförd studie presenterad i Naturenergi , ett team av forskare vid Technion-Israel Institute of Technology har tagit itu med några av dessa utmaningar, presenterar en ny teknik för att klyva vatten som kan förbättra befintliga metoder för elektrolytisk väteproduktion. Deras forskning hämtar inspiration från en av deras tidigare studier om fotoelektrokemisk (PEC) vattendelning, där de försökte kombinera solenergi och vatten(foto)elektrolys för att generera väte från solljus och vatten.
En av de största utmaningarna som beskrivits i detta tidigare arbete var insamlingen av vätgas från miljontals PEC-celler distribuerade i solfältet. I sin studie, de Technion-baserade forskarna försökte utveckla en teknik som effektivt kunde tackla denna utmaning.
"Att ta solcellsanläggningar (PV) som basscenario, solfarmen består av miljontals individuella PV-celler, där strömmen (och spänningen) samlas in från var och en av dem till ett metallnät, "Avner Rothschild, en av forskarna som genomförde studien, berättade för TechXplore. "Det här är enkelt med el, men inte så med vätgas."
I en idealisk PEC solcellsanläggning för framtiden, PV-celler skulle ersättas av PEC-celler, som kan producera väte i en komponent som kallas katodrum, och syre i en separat kammare som kallas anodfack. Dessa två fack bör separeras, åtminstone genom ett membran, för att säkerställa att väte och syre inte blandas, eftersom detta skulle orsaka en explosion. Dessutom, vätgasen måste samlas upp från varje enskild cell.
Att skapa denna installation har hittills visat sig vara tekniskt svårt och dyrt, eftersom det kräver en mycket kostsam rörledning. I sista hand, detta har gjort förverkligandet av lösningar för storskalig väteproduktion genom PEC-vattenklyvning orealistiskt.
"Vi sökte en väg ut ur denna utmaning, och kom på idén att separera syre- och väteavdelningarna i PEC-cellen i två separata celler, så att syret genereras i solfältet och släpps ut i atmosfären, medan vätet genereras i en central reaktor i hörnet av fältet, " Sa Rothschild. "Separationen i två celler är möjlig genom att sätta in ytterligare en uppsättning av två elektroder, kallade hjälpelektroder, som laddas och urladdas samtidigt av OH - joner som är involverade i vattenspjälkningsreaktionen, förmedlar därigenom jonbytet mellan de två cellerna (vilket är nödvändigt för att stänga den elektriska kretsen)."
I deras tidigare tidning, publiceras i Naturmaterial , Rothschild och hans kollegor presenterade en störande ny metod för vattenelektrolys (elektrolysatorer) och fotoelektrolys (PEC) arkitekturer. Detta lovande tillvägagångssätt, dock, introducerade ytterligare en utmaning med att regenerera hjälpelektroderna när de blir mättade i slutet av en produktionscykel. Forskarna föreslog att elektroderna kunde bytas ut i slutet av varje cykel, men detta skulle vara ganska besvärligt, så de fortsatte att utforska alternativa lösningar.
"Vi upptäckte då att när du värmer hjälpelektroden i vätecellen, efter att den laddats (för att bli NiOOH), det frigör syrgasbubblor spontant och regenererar till sitt initiala tillstånd (Ni(OH) 2 ), " Sa Rothschild. "Denna upptäckt ledde till utvecklingen av E-TAC-vattenklyvningsprocessen som presenteras i detta arbete."
E-TAC, den nya vattenklyvningstekniken som föreslagits av Rothschild och hans kollegor, har en hög energieffektivitet på 98,7 procent, därför överträffar den avsevärt konventionella elektrolysatorer, som vanligtvis har en energieffektivitet på ~70 till 80 procent för toppmoderna enheter. En ytterligare fördel med E-TAC är att den producerar väte och syre sekventiellt, medan i de flesta andra elektrolysatorer, de produceras samtidigt. Detta tar slutligen bort behovet av ett membran som separerar vätgas och syrgas, vilket avsevärt förenklar konstruktionen och monteringen av cellerna, samt deras drift och underhåll.
"Potentiellt, detta kan leda till stora besparingar på kapital- och driftskostnader, leder till utvecklingen av kostnadseffektiv vattenklyvningsteknik som kan konkurrera med SMR (ångmetanreformering), erbjuder billigt väte utan CO 2 utsläpp, förutsatt att elen kommer från förnybara källor såsom vattenkraft, sol- eller vindkraft, " sa Rothschild.
Vid konventionell vattenelektrolys, väte och syre produceras alltid samtidigt i katod- och anodavdelningarna, respektive. Facken är placerade så nära varandra som möjligt, för att minimera elektriska ohmska förluster, och de är åtskilda av ett membran för att undvika skapandet av ett explosivt H 2 /O 2 blandning.
"Katoden reducerar vatten, genererar väte (H 2 molekyler) och hydroxidjoner (OH - ) genom en reaktion som kallas HER (väteutvecklingsreaktion), " Sa Rothschild. "OH - joner migrerar till anoden genom elektrolyten och genom membranet, där de oxideras genom OER (oxygen evolution reaction). Tillsammans, dessa två reaktioner (HER och OER) fullbordar vattenspjälkningsreaktionen:2H 2 O 2H 2 + O 2 ."
Vid konventionell vattenelektrolys, de två elektrokemiska reaktionerna som beskrivs av Rothschild är kopplade i både tid och rum, eftersom de inträffar samtidigt, i samma cell och i närheten. Dessutom, dessa egenskaper är desamma oavsett om processen tillämpas på alkaliska eller PEM-elektrolysatorer.
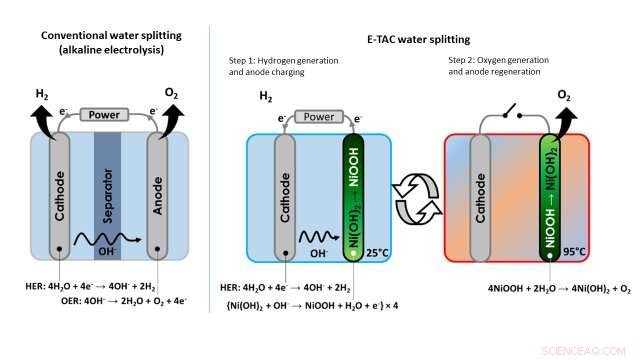
Bild som visar skillnaden mellan det konventionella tillvägagångssättet för vattendelning (alkalisk elektrolys) och E-TAC-tekniken för vattendelning som föreslagits av forskarna. Kredit:Dotan et al.
Till skillnad från denna traditionella metod för vattenelektrolys, den vattenklyvningsprocessen som forskarna utarbetat frikopplar HER- och OER-reaktionerna, som istället förekommer vid olika tidpunkter och potentiellt i olika delar av en enhet. Istället för att vara kontinuerlig, därför, E-TAC kan beskrivas som en "batchprocess" med två cykler, den första genererar väte elektrokemiskt och den andra syre via en spontan kemisk reaktion.
"Vi placerar katoden (samma katod som används i alkalisk elektrolys) och anoden (som skiljer sig från anoden vid konventionell elektrolys) i en elektrolyscell och skickar ström mellan dem, " sa Rothschild. "Katoden genererar väte genom HER-reaktionen, precis som det gör i det konventionella vattenelektrolysfallet, men anoden gör en helt annan sak. Anoden laddas i huvudsak genom att absorbera OH - joner som genereras vid katoden, och transformerar gradvis från Ni(OH) 2 (nickelhydroxid) till NiOOH (nickeloxihydroxid)."
Intressant, reaktionen som produceras i anoden är densamma som sker vid katoden på alkaliska batterier (t.ex. Ni-MH-batterier) medan de laddas. Detta tyder på att det kan fungera bra i många cykler, precis som det gör i alkaliska batterier.
Ibland, dock, laddningen av anoden i E-TAC-processen måste avbrytas, för om den blir överladdad, det kan börja generera syre. När laddningen går över en viss nivå, därför, forskarna måste begränsa spänningen som appliceras på cellerna för att undvika eventuella explosioner som härrör från samgenerering av syre och väte.
"In order to continue the E-TAC process, we then need to regenerate the charged anode (NiOOH) back to its initial state (Ni(OH) 2 ), " Rothschild explained. "We do so by raising its temperature, thereby accelerating the rate of the spontaneous chemical reaction between the charged anode and water, which releases oxygen and regenerates the anode back to its initial state."
The technique devised by Rothschild and his colleagues thus entails the use of heat to control the chemical reaction that generates oxygen, as the rate of the reaction slows down at low temperatures and accelerates at high temperatures. The generation of hydrogen occurs at a low or ambient temperature, and the generation of oxygen at high temperatures around 95 degrees Celsius. This is why the researchers decided to call it the E-TAC process, which stands for electrochemical-thermally activated chemical process.
"In the proof-of-concept lab tests presented in our article, we manually moved the anode from the cold cell (i.e. a glass beaker filled with alkaline aqueous solution at ambient temperature) to the hot cell (i.e. the same type of beaker, but heated to 95 degrees Celsius), so the separation between hydrogen and oxygen generation was not only in time but also in place, " Rothschild explained. "However, in a real-world industrial system, we foresee a different scenario in which the two electrodes (anode and cathode) and stationary (not moving), whereas the cell in which they are is filled sequentially with cold or hot electrolyte solutions."
Separating the production of hydrogen and oxygen, which removes the need for a membrane separating the two different chambers inside electrolytic cells, results in substantial savings over traditional electrolysis approaches. Faktiskt, sealing the membrane is generally expensive and also complicates the overall production process. The membrane in conventional systems requires high-purity water and ongoing maintenance, all of which are unnecessary in E-TAC.
Dessutom, the technique devised by Rothschild and his colleagues entirely eliminates the risk of volatile encounters between oxygen and hydrogen, as well as resulting explosions. In traditional systems, å andra sidan, this risk is still present, as the membrane could rip or its seal could break.
"Currently, the use of membranes also limits the pressure in hydrogen production, " Rothschild said. "E-TAC renders the membrane unnecessary, thus facilitating hydrogen production under much higher pressure and eliminating some of the high costs of compressing the hydrogen later. Dessutom, in the new process we proposed, oxygen is produced via a spontaneous chemical reaction between the charged anode and the water, without using an electrical current. This reaction eliminates the need for electricity during oxygen production and increases energetic efficiency from ~70 to 80 percent using customary methods to an unprecedented 98.7 percent."
The technique developed by Rothschild and his colleagues could lower operating costs of sustainable hydrogen production and equipment costs. The researchers have estimated that the production costs for equipment based on E-TAC would be approximately half of those for existing technologies.
"The process we invented presents a conceptual breakthrough in water splitting, and in view of the advantages it offers, it may become a game-changer and lead to a new technology for hydrogen production from water without CO 2 utsläpp, which could compete with SMR to produce clean hydrogen and enable the transition from fossil fuels to clean hydrogen fuel, " Rothschild said.
After they finished writing their paper, the researchers at Technion patented their invention and founded a start-up called H 2 Pro, with the mission of developing and distributing new water splitting technology based on the E-TAC technique. They hope to soon commercialize this technology by scaling-up the electrodes and cells used in their study, constructing and testing hydrogen generators based on the E-TAC water-splitting process, optimizing their operation scheme and examining high-pressure hydrogen production.
"We also plan to carry out further academic research to study new electrode materials and apply advanced analytical methods to understand the correlations between electrode composition and microstructure and its function properties, in order to develop the next generation of Ni(OH) 2 -based electrodes for our E-TAC water-splitting process, " Rothschild said. "Our goal is to improve their capacity (so that we can run longer processes) with fast charging and regeneration rates to enable high hydrogen production rates."
© 2019 Science X Network