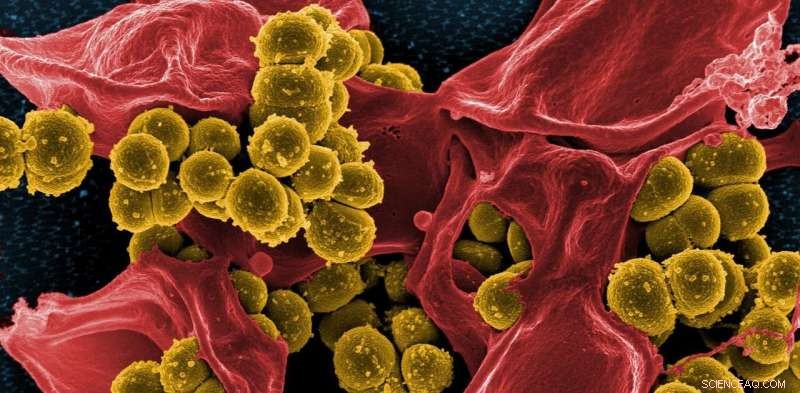
En färgad elektronmikroskopbild av MRSA. Kredit:NIH - NIAID/flickr, CC BY
Föreställ dig att du är en fossiljägare. Du tillbringar månader i Arizonas hetta och gräver upp ben bara för att upptäcka att det du har upptäckt är från en tidigare upptäckt dinosaurie.
Så har sökandet efter antibiotika slagit ut den senaste tiden. De relativt få antibiotikajägarna där ute fortsätter att hitta samma typer av antibiotika.
Med den snabba ökningen av läkemedelsresistens hos många patogener, nya antibiotika behövs i desperat behov. Det kan bara vara en tidsfråga innan ett sår eller en repa blir livshotande. Ändå har få nya antibiotika kommit in på marknaden på senare tid, och även dessa är bara mindre varianter av gamla antibiotika.
Även om utsikterna ser dystra ut, den senaste revolutionen inom artificiell intelligens (AI) ger nytt hopp. I en studie publicerad den 20 februari i tidskriften Cell , forskare från MIT och Harvard använde en typ av AI som kallas djupinlärning för att upptäcka nya antibiotika.
Det traditionella sättet att upptäcka antibiotika – från jord eller växtextrakt – har inte avslöjat nya kandidater, och det finns många sociala och ekonomiska hinder för att lösa detta problem, också. Vissa forskare har nyligen försökt ta itu med det genom att söka i bakteriers DNA efter nya antibiotikaproducerande gener. Andra letar efter antibiotika på exotiska platser som i våra näsor.
Läkemedel som hittats med sådana okonventionella metoder möter en stenig väg för att nå marknaden. De läkemedel som är effektiva i en petriskål kanske inte fungerar bra inuti kroppen. De kan inte absorberas bra eller kan ha biverkningar. Att tillverka dessa läkemedel i stora kvantiteter är också en betydande utmaning.
Djup lärning
Gå in i djupinlärning. Dessa algoritmer driver många av dagens ansiktsigenkänningssystem och självkörande bilar. De efterliknar hur neuroner i våra hjärnor fungerar genom att lära sig mönster i data. En individuell artificiell neuron - som en minisensor - kan upptäcka enkla mönster som linjer eller cirklar. Genom att använda tusentals av dessa artificiella neuroner, djupinlärning AI kan utföra extremt komplexa uppgifter som att känna igen katter i videor eller upptäcka tumörer i biopsibilder.
Med tanke på dess kraft och framgång, det kanske inte är förvånande att lära sig att forskare som letar efter nya läkemedel anammar djupinlärning AI. Men att bygga en AI-metod för att upptäcka nya läkemedel är ingen trivial uppgift. Till stor del, detta beror på att det inte finns någon gratis lunch inom AI.
No Free Lunch-satsen säger att det inte finns någon universellt överlägsen algoritm. Detta innebär att om en algoritm fungerar spektakulärt i en uppgift, säg ansiktsigenkänning, då kommer det att misslyckas spektakulärt i en annan uppgift, som drogupptäckt. Därför kan forskare inte bara använda off-the-shelf djupinlärning AI.
Harvard-MIT-teamet använde en ny typ av djupinlärning AI som kallas grafiska neurala nätverk för läkemedelsupptäckt. Tillbaka i AI-stenåldern 2010, AI-modeller för läkemedelsupptäckt byggdes med hjälp av textbeskrivningar av kemikalier. Det är som att beskriva en persons ansikte med ord som "mörka ögon" och "lång näsa". Dessa textbeskrivningar är användbara men målar uppenbarligen inte upp hela bilden. AI-metoden som används av Harvard-MIT-teamet beskriver kemikalier som ett nätverk av atomer, vilket ger algoritmen en mer komplett bild av kemikalien än vad textbeskrivningar kan ge.
Människokunskap och AI blanka blad
Men enbart djupinlärning är inte tillräckligt för att upptäcka nya antibiotika. Det måste kombineras med djup biologisk kunskap om infektioner.
Harvard-MIT-teamet tränade noggrant AI-algoritmen med exempel på läkemedel som är effektiva och de som inte är det. Dessutom, de använde läkemedel som är kända för att vara säkra för människor för att träna AI. De använde sedan AI-algoritmen för att identifiera potentiellt säkra men ändå potenta antibiotika från miljontals kemikalier.
Till skillnad från människor, AI har inga förutfattade meningar, speciellt om hur ett antibiotikum ska se ut. Använder gammaldags AI, mitt labb upptäckte nyligen några överraskande kandidater för behandling av tuberkulos, inklusive ett antipsykotiskt läkemedel. I en studie av Harvard-MIT-teamet, de hittade en guldgruva av nya kandidater. Dessa läkemedelskandidater ser inte ut som existerande antibiotika. En lovande kandidat är Halicin, ett läkemedel som undersöks för att behandla diabetes.
halicin, förvånande, var potent inte bara emot E coli , bakterierna som AI-algoritmen tränades på, men också på mer dödliga patogener, inklusive de som orsakar tuberkulos och koloninflammation. I synnerhet, Halicin var potent mot läkemedelsresistenta Acinetobacter baumanni . Denna bakterie toppar listan över mest dödliga patogener som sammanställts av Centers for Disease Control and Prevention.
Tyvärr, Halicins breda styrka tyder på att det också kan förstöra ofarliga bakterier i vår kropp. Det kan också ha metabola biverkningar, eftersom det ursprungligen utformades som ett läkemedel mot diabetes. Med tanke på det trängande behovet av nya antibiotika, dessa kan vara små uppoffringar att betala för att rädda liv.
Att ligga före evolutionen
Med tanke på löftet om Halicin, ska vi stoppa sökandet efter nya antibiotika?
Halicin kan komma över alla hinder och så småningom nå marknaden. Men det måste fortfarande övervinna en obönhörlig fiende som är huvudorsaken till läkemedelsresistenskrisen:evolutionen. Människor har kastat många droger på patogener under det senaste århundradet. Ändå har patogener alltid utvecklat resistens. Så det skulle troligen inte dröja länge innan vi stöter på en halicinresistent infektion. Ändå, med kraften av djupinlärning AI, vi kan nu vara bättre lämpade att snabbt svara med ett nytt antibiotikum.
Många utmaningar ligger framför potentiella antibiotika som upptäckts med hjälp av AI för att nå kliniken. Tillstånden under vilka dessa läkemedel testas skiljer sig från dem som finns inuti människokroppen. Nya AI-verktyg byggs av mitt labb och andra för att simulera kroppens inre miljö för att bedöma antibiotikastyrkan. AI-modeller kan nu också förutsäga läkemedelstoxicitet och biverkningar. Dessa AI-tekniker tillsammans kan snart ge oss ett ben i den oändliga kampen mot läkemedelsresistens.
Den här artikeln är återpublicerad från The Conversation under en Creative Commons-licens. Läs originalartikeln. 